| SPTB |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 1S35, 3EDU, 3F57, 3KBT, 3KBU, 3LBX | | |
| Ідентифікатори |
|---|
| Символи | SPTB, EL3, HS2, HSPTB1, SPH2, spectrin beta, erythrocytic |
|---|
| Зовнішні ІД | OMIM: 182870 MGI: 98387 HomoloGene: 295 GeneCards: SPTB |
|---|
| |
| Пов'язані генетичні захворювання |
|---|
| ожиріння, hereditary spherocytosis type 2[1] |
| Онтологія гена |
|---|
| Молекулярна функція | • actin filament binding
• structural constituent of cytoskeleton
• GO:0001948, GO:0016582 protein binding
• ankyrin binding
• actin binding
|
|---|
| Клітинна компонента | • spectrin
• intrinsic component of the cytoplasmic side of the plasma membrane
• cell surface
• cell cortex
• actin cytoskeleton
• spectrin-associated cytoskeleton
• цитоскелет
• цитоплазма
• комплекс Ґольджі
• гіалоплазма
• GO:0009327 protein-containing complex
|
|---|
| Біологічний процес | • MAPK cascade
• axon guidance
• endoplasmic reticulum to Golgi vesicle-mediated transport
• actin filament capping
• cytoskeleton organization
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|

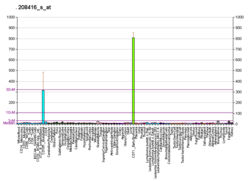 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_000347
NM_001024858
NM_001355436
NM_001355437 |
| |
|---|
| RefSeq (білок) | | NP_001020029
NP_001342365
NP_001342366 |
| |
|---|
| Локус (UCSC) | Хр. 14: 64.75 – 64.88 Mb | Хр. 12: 76.63 – 76.76 Mb |
|---|
| PubMed search | [2] | [3] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
SPTB (англ. Spectrin beta, erythrocytic) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 14-ї хромосоми.[4] Довжина поліпептидного ланцюга білка становить 2 137 амінокислот, а молекулярна маса — 246 468[5].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MTSATEFENV | | GNQPPYSRIN | | ARWDAPDDEL | | DNDNSSARLF | | ERSRIKALAD |
| EREVVQKKTF | | TKWVNSHLAR | | VSCRITDLYK | | DLRDGRMLIK | | LLEVLSGEML |
| PKPTKGKMRI | | HCLENVDKAL | | QFLKEQRVHL | | ENMGSHDIVD | | GNHRLVLGLI |
| WTIILRFQIQ | | DIVVQTQEGR | | ETRSAKDALL | | LWCQMKTAGY | | PHVNVTNFTS |
| SWKDGLAFNA | | LIHKHRPDLI | | DFDKLKDSNA | | RHNLEHAFNV | | AERQLGIIPL |
| LDPEDVFTEN | | PDEKSIITYV | | VAFYHYFSKM | | KVLAVEGKRV | | GKVIDHAIET |
| EKMIEKYSGL | | ASDLLTWIEQ | | TITVLNSRKF | | ANSLTGVQQQ | | LQAFSTYRTV |
| EKPPKFQEKG | | NLEVLLFTIQ | | SRMRANNQKV | | YTPHDGKLVS | | DINRAWESLE |
| EAEYRRELAL | | RNELIRQEKL | | EQLARRFDRK | | AAMRETWLSE | | NQRLVAQDNF |
| GYDLAAVEAA | | KKKHEAIETD | | TAAYEERVRA | | LEDLAQELEK | | ENYHDQKRIT |
| ARKDNILRLW | | SYLQELLQSR | | RQRLETTLAL | | QKLFQDMLHS | | IDWMDEIKAH |
| LLSAEFGKHL | | LEVEDLLQKH | | KLMEADIAIQ | | GDKVKAITAA | | TLKFTEGKGY |
| QPCDPQVIQD | | RISHLEQCFE | | ELSNMAAGRK | | AQLEQSKRLW | | KFFWEMDEAE |
| SWIKEKEQIY | | SSLDYGKDLT | | SVLILQRKHK | | AFEDELRGLD | | AHLEQIFQEA |
| HGMVARKQFG | | HPQIEARIKE | | VSAQWDQLKD | | LAAFCKKNLQ | | DAENFFQFQG |
| DADDLKAWLQ | | DAHRLLSGED | | VGQDEGATRA | | LGKKHKDFLE | | ELEESRGVME |
| HLEQQAQGFP | | EEFRDSPDVT | | HRLQALRELY | | QQVVAQADLR | | QQRLQEALDL |
| YTVFGETDAC | | ELWMGEKEKW | | LAEMEMPDTL | | EDLEVVQHRF | | DILDQEMKTL |
| MTQIDGVNLA | | ANSLVESGHP | | RSREVKQYQD | | HLNTRWQAFQ | | TLVSERREAV |
| DSALRVHNYC | | VDCEETSKWI | | TDKTKVVEST | | KDLGRDLAGI | | IAIQRKLSGL |
| ERDVAAIQAR | | VDALERESQQ | | LMDSHPEQKE | | DIGQRQKHLE | | ELWQGLQQSL |
| QGQEDLLGEV | | SQLQAFLQDL | | DDFQAWLSIT | | QKAVASEDMP | | ESLPEAEQLL |
| QQHAGIKDEI | | DGHQDSYQRV | | KESGEKVIQG | | QTDPEYLLLG | | QRLEGLDTGW |
| NALGRMWESR | | SHTLAQCLGF | | QEFQKDAKQA | | EAILSNQEYT | | LAHLEPPDSL |
| EAAEAGIRKF | | EDFLGSMENN | | RDKVLSPVDS | | GNKLVAEGNL | | YSDKIKEKVQ |
| LIEDRHRKNN | | EKAQEASVLL | | RDNLELQNFL | | QNCQELTLWI | | NDKLLTSQDV |
| SYDEARNLHN | | KWLKHQAFVA | | ELASHEGWLE | | NIDAEGKQLM | | DEKPQFTALV |
| SQKLEALHRL | | WDELQATTKE | | KTQHLSAARS | | SDLRLQTHAD | | LNKWISAMED |
| QLRSDDPGKD | | LTSVNRMLAK | | LKRVEDQVNV | | RKEELGELFA | | QVPSMGEEGG |
| DADLSIEKRF | | LDLLEPLGRR | | KKQLESSRAK | | LQISRDLEDE | | TLWVEERLPL |
| AQSADYGTNL | | QTVQLFMKKN | | QTLQNEILGH | | TPRVEDVLQR | | GQQLVEAAEI |
| DCQDLEERLG | | HLQSSWDRLR | | EAAAGRLQRL | | RDANEAQQYY | | LDADEAEAWI |
| GEQELYVISD | | EIPKDEEGAI | | VMLKRHLRQQ | | RAVEDYGRNI | | KQLASRAQGL |
| LSAGHPEGEQ | | IIRLQGQVDK | | HYAGLKDVAE | | ERKRKLENMY | | HLFQLKRETD |
| DLEQWISEKE | | LVASSPEMGQ | | DFDHVTLLRD | | KFRDFARETG | | AIGQERVDNV |
| NAFIERLIDA | | GHSEAATIAE | | WKDGLNEMWA | | DLLELIDTRM | | QLLAASYDLH |
| RYFYTGAEIL | | GLIDEKHREL | | PEDVGLDAST | | AESFHRVHTA | | FERELHLLGV |
| QVQQFQDVAT | | RLQTAYAGEK | | AEAIQNKEQE | | VSAAWQALLD | | ACAGRRTQLV |
| DTADKFRFFS | | MARDLLSWME | | SIIRQIETQE | | RPRDVSSVEL | | LMKYHQGINA |
| EIETRSKNFS | | ACLELGESLL | | QRQHQASEEI | | REKLQQVMSR | | RKEMNEKWEA |
| RWERLRMLLE | | VCQFSRDASV | | AEAWLIAQEP | | YLASGDFGHT | | VDSVEKLIKR |
| HEAFEKSTAS | | WAERFAALEK | | PTTLELKERQ | | IAERPAEETG | | PQEEEGETAG |
| EAPVSHHAAT | | ERTSPVSLWS | | RLSSSWESLQ | | PEPSHPY |
Кодований геном білок за функціями належить до кепінгів актину, фосфопротеїнів. Задіяний у такому біологічному процесі, як альтернативний сплайсинг. Білок має сайт для зв'язування з молекулою актину. Локалізований у цитоплазмі, цитоскелеті.
Література
- Yoon S.H., Kentros C.G., Prchal J.T. (1990). Identification of an unusual deletion within homologous repeats of human reticulocyte beta-spectrin and probable peptide polymorphism. Gene. 91: 297—302. PMID 1976574 DOI:10.1016/0378-1119(90)90104-Y
- Speicher D.W., Marchesi V.T. (1984). Erythrocyte spectrin is comprised of many homologous triple helical segments. Nature. 311: 177—180. PMID 6472478 DOI:10.1038/311177a0
- Tang H.Y., Speicher D.W. (2004). In vivo phosphorylation of human erythrocyte spectrin occurs in a sequential manner. Biochemistry. 43: 4251—4262. PMID 15065869 DOI:10.1021/bi036092x
- Maciag M., Plochocka D., Adamowicz-Salach A., Burzynska B. (2009). Novel beta-spectrin mutations in hereditary spherocytosis associated with decreased levels of mRNA. Br. J. Haematol. 146: 326—332. PMID 19538529 DOI:10.1111/j.1365-2141.2009.07759.x
- Kusunoki H., MacDonald R.I., Mondragon A. (2004). Structural insights into the stability and flexibility of unusual erythroid spectrin repeats. Structure. 12: 645—656. PMID 15062087 DOI:10.1016/j.str.2004.02.022
- Maillet P., Alloisio N., Morle L., Delaunay J. (1996). Spectrin mutations in hereditary elliptocytosis and hereditary spherocytosis. Hum. Mutat. 8: 97—107. PMID 8844207 DOI:10.1002/(SICI)1098-1004(1996)8:2<97::AID-HUMU1>3.3.CO;2-W
Примітки
- ↑ Захворювання, генетично пов'язані з SPTB переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:11274 (англ.) . Процитовано 11 вересня 2017.
{{cite web}}: Обслуговування CS1: Сторінки з параметром url-status, але без параметра archive-url (посилання) - ↑ UniProt, P11277 (англ.) . Архів оригіналу за 21 жовтня 2017. Процитовано 11 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| Людські | Мікрофіламенти
та актин-зв'язуючі білки | | Міофіламенти | | Актин | |
|---|
| Міозин | - I
- II
- III
- V
- VI
- VII
- IX
- X
- XV
- XVIII
- Легкий ланцюг міозину
|
|---|
| Інші | |
|---|
|
|---|
| Інші | |
|---|
|
|---|
| Проміжні філаменти | Тип 1/2
(Кератин,
Цитокератин) | Епітеліальні кератини
(м'які альфа-кератини) | - тип I/хромосома 17
- хромосома 12
- інші
|
|---|
Кератини волосся
(жорсткі альфа-кератини) | |
|---|
| Незгруповані альфа | |
|---|
| Не-альфа | |
|---|
|
|---|
| Тип 3 | |
|---|
| Тип 4 | - Інтернексин
- Нестин
- Нейрофіламент
- Синемін
- Синкоїлін
|
|---|
| Тип 5 | |
|---|
|
|---|
Мікротрубочки
та пов'язані білки | |
|---|
| Катеніни | |
|---|
| Мембранні | |
|---|
| Інші | |
|---|
|
|---|
| Нелюдські | |
|---|















