Triisobutylaluminium
| Triisobutylaluminium | |||
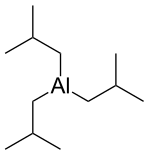 | |||
| Structure du triisobutylaluminium | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | tris(2-méthylpropyl)alumane | ||
| No CAS | 100-99-2 | ||
| No ECHA | 100.002.643 | ||
| No CE | 202-906-3 | ||
| PubChem | 16682931 | ||
| SMILES | CC(C)C[Al](CC(C)C)CC(C)C PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/3C4H9.Al/c3*1-4(2)3;/h3*4H,1H2,2-3H3; Std. InChIKey : MCULRUJILOGHCJ-UHFFFAOYSA-N | ||
| Apparence | liquide incolore[1] | ||
| Propriétés chimiques | |||
| Formule | C12H27Al((CH3)2CHCH2)3Al | ||
| Masse molaire[2] | 198,324 3 ± 0,011 5 g/mol C 72,67 %, H 13,72 %, Al 13,6 %, | ||
| Propriétés physiques | |||
| Masse volumique | 0,782 g/cm3[1] à 20 °C | ||
| Précautions | |||
| SGH[1] | |||
    Danger H225 : Liquide et vapeurs très inflammables H250 : S'enflamme spontanément au contact de l'air H260 : Dégage, au contact de l'eau, des gaz inflammables qui peuvent s'enflammer spontanément H304 : Peut être mortel en cas d'ingestion et de pénétration dans les voies respiratoires H314 : Provoque de graves brûlures de la peau et des lésions oculaires H336 : Peut provoquer somnolence ou vertiges H361f : Susceptible de nuire à la fertilité. H373 : Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H411 : Toxique pour les organismes aquatiques, entraîne des effets à long terme EUH014 : Réagit violemment au contact de l'eau P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P231+P232 : Manipuler sous gaz inerte. Protéger de l’humidité. P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin. P301+P330+P331 : En cas d'ingestion : rincer la bouche. NE PAS faire vomir. P303+P361+P353 : En cas de contact avec la peau (ou les cheveux) : enlever immédiatement les vêtements contaminés. Rincer la peau à l’eau/se doucher. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P335+P334 : Enlever avec précaution les particules déposées sur la peau. Rincer à l’eau fraîche/poser une compresse humide. | |||
| NFPA 704[1] | |||
4 3 2 | |||
| Transport[1] | |||
Numéro ONU : 3394 : MATIÈRE ORGANO-MÉTALLIQUE LIQUIDE PYROPHORIQUE, HYDRORÉACTIVE Étiquettes :  4.2 : Matières sujettes à l'inflammation spontanée  4.3 : Matières qui, au contact de l'eau, dégagent des gaz inflammables Emballage : Groupe d'emballage I : matières très dangereuses ; | |||
| Écotoxicologie | |||
| LogP | 4,11[1] (octanol/eau) pour le solvant hexane | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le triisobutylaluminium, ou TiBA, est un composé organoaluminique de formule chimique ((CH3)2CHCH2)3Al. Il s'agit d'un liquide incolore pyrophorique qui réagit violemment avec l'eau, les alcools, l'oxygène, les oxydants, les acides et les bases. Il réagit également avec les aldéhydes et les cétones[3]. Il est utilisé essentiellement pour produire des alcools primaires et des alcènes terminaux[4].
Le triisobutylaluminium existe en équilibre avec son dimère, selon une constante de dissociation KD qui vaut 3,810 à 20 °C[5] :
- 2 ((CH3)2CHCH2)3Al [((CH3)2CHCH2)3Al]2.
Dans le dimère, la liaison carbone–aluminium est allongée et montre des indications d'une rotation restreinte. Par souci de simplification, on décrira le TiBA comme monomère dans cette page.
Production
Les composés trialkylaluminium sont produits industriellement en faisant réagir de la poudre d'aluminium, de l'hydrogène H2 et les alcènes souhaités. La synthèse du triisobutylaluminium se déroule en deux étapes. La première donne l'hydrure de diisobutylaluminium ((CH3)2CHCH2)2AlH à partir de l'isobutylène CH2=C(CH3)2 :
- 4 CH2=C(CH3)2 + 2 Al + 3 H2 ⟶ 2 ((CH3)2CHCH2)2AlH.
Une seconde étape consiste en l'addition supplémentaire d'isobutylène pour aboutir au triisobutylaluminium :
- CH2=C(CH3)2 + ((CH3)2CHCH2)2AlH ⟶ ((CH3)2CHCH2)3Al.
Réactions
Les alcènes terminaux sont rapidement éliminés des composés trialkylaluminium β-ramifiés. Les composés trialkylaluminium sont employés dans l'industrie pour la production de polymères. Le triisobutylaluminium est l'un de ces composés les plus courants et présente un taux de liaisons Al–H significatif à l'équilibre. La plus grande stabilité des composés trialkylaluminium linéaires par rapport aux ramifiés est à la base de l'obtention de composés trialkylaluminium linéaires à partir du triisobutylaluminium :
- ((CH3)2CHCH2)3Al + 3 RCH=CH2 ⟶ (RCH2CH2)3Al + 3 CH2=C(CH3)2.
Notes et références
- ↑ a b c d e et f « Fiche du composé Triisobutylaluminum, 25% w/w in hexane », sur Alfa Aesar (consulté le ).
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Pradyot Patnaik, A Comprehensive Guide to the Hazardous Properties of Chemical Substances, John Wiley & Sons, 2007, p. 607. (ISBN 0-470-13494-1)
- ↑ (en) Michael J. Krause, Frank Orlandi, Alfred T. Saurage et Joseph R. Zietz Jr., « Aluminum Compounds, Organic », Ullmann's Encyclopedia of Industrial Chemistry, (DOI 10.1002/14356007.a01_543, lire en ligne)
- ↑ (en) Martin B. Smith, « The monomer-dimer equilibria of liquid aluminum alkyls: II. Triisobutylaluminum », Journal of Organometallic Chemistry, vol. 22, no 2, , p. 273-281 (DOI 10.1016/S0022-328X(00)86043-X, lire en ligne)
v · m | |||||
|---|---|---|---|---|---|
| Al(I) | |||||
| Al(II) |
| ||||
| Al(III) |
| ||||
 Portail de la chimie
Portail de la chimie











 Triisobutylaluminium
Triisobutylaluminium