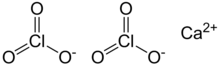
Kalsiyum klorat
 | |
| Adlandırmalar | |
|---|---|
Kalsiyum diklorat | |
Diğer adlar Kalsiyum klorat dihidrat | |
| Tanımlayıcılar | |
| |
3D model (JSmol) |
|
| ChemSpider |
|
| ECHA InfoCard | 100.030.331 |
| EC Numarası |
|
PubChem CID |
|
| RTECS numarası |
|
CompTox Bilgi Panosu (EPA) |
|
InChI
| |
SMILES
| |
| Özellikler | |
| Molekül formülü | Ca(ClO3)2 |
| Molekül kütlesi | 206.98 gr/mol |
| Görünüm | havadan nem çekerek sulanan beyaz katı |
| Koku | kokusuz |
| Yoğunluk | 2.71 gr/cm3 |
| Erime noktası | 325 °C |
| Çözünürlük (su içinde) | 209 gr/100mL (20 °C) 197 gr/100mL (25 °C) |
| Yapı | |
| monoklinik | |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |  |
| İşaret sözcüğü | Tehlike |
| Tehlike ifadeleri | H272 |
| NFPA 704 (yangın karosu) |  1 0 1 OX |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 4500 mg/kg (oral, sıçan)[1] |
| Benzeyen bileşikler | |
Diğer anyonlar | Kalsiyum klorür Kalsiyum bromat Kalsiyum bromür |
Diğer katyonlar | Potasyum klorat Sodyum klorat Baryum klorat Magnezyum klorat |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
| Bilgi kutusu kaynakları | |
Kalsiyum klorat kimyasal formülü Ca(ClO3)2 olan bir bileşiktir. Klorik asitin kalsiyum tuzudur. Potasyum klorat gibi, kuvvetli bir oksitleyici olan bu bileşik, piroteknik formülasyonlarda kullanılabilir. Kalsiyum klorat kuvvetle ısıtıldığında ya da organik madde gibi indirgeyici maddelerle karıştırıldığında patlayabilir.
Kalsiyum klorat, kalsiyum klorürün kuvvetli bir oksitleyici madde ile yükseltgenmesiyle oluşturulabilir.[2]












