Natrijum tiosulfat
| Natrijum-tiosulfat | |||
|---|---|---|---|
 | |||
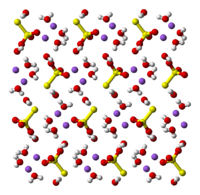 | |||
| IUPAC ime |
| ||
| Drugi nazivi | Natrijum-hiposulfat (čest naziv u fotografiji) Hiposulfat sode | ||
| Identifikacija | |||
| CAS registarski broj | 7772-98-7  Y, 10102-17-7 (pentahidrat) Y, 10102-17-7 (pentahidrat)  Y Y | ||
| PubChem[1][2] | 24477 | ||
| ChemSpider[3] | 22885  Y Y | ||
| UNII | L0IYT1O31N  Y Y | ||
| MeSH | Sodium+thiosulfate | ||
| ChEMBL[4] | CHEMBL2096650  Y Y | ||
| RTECS registarski broj toksičnosti | XN6476000 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | Na2S2O3 | ||
| Molarna masa | 158.09774 g/mol | ||
| Agregatno stanje | beli kristali | ||
| Gustina | 1.667 g/cm³, osnovno | ||
| Tačka topljenja | 48.3 °C | ||
| Tačka ključanja | Razlaže se | ||
| Rastvorljivost u vodi | veoma rastvoran | ||
| Baznost (pKb) | N/A | ||
| Struktura | |||
| Geometrija molekula | tetraedar-anion | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS | ||
| EU-klasifikacija | Nije toksičan | ||
| NFPA 704 |  0 1 0 | ||
| R-oznake | R35 | ||
| S-oznake | (S1/2) S26 S37/39 S45 | ||
| Tačka paljenja | Nije zapaljiv | ||
|
| |||
| Infobox references | |||
Natrijum-tiosulfat je hemijsko neorgansko jedinjenje hemijske formule Na2S2O3.
Dobijanje
U laboratoriji se dobija zagrevanjem rastvora natrijum-sulfita sa elementarnim sumporom:
- Na2SO3 + S → Na2S2O3
Ukoliko se ova reakcija izvodi sa radioaktivnim izotopom sumpora, pa se onda deluje kiselinom na dobijeni radioaktivni natrijum-tiosulfat, sav elementarni sumpor koji se dobije će biti radioaktivan, dok sumpor-dioksid koji se oslobađa to neće biti. Ovo navodi na zaključak da dva sumporova atoma u natrijum-tiosulfatu nisu ekvivalentna.[5]
Nekada su se veće količine ove soli dobijale iz kalcijum-sulfida koji bi ostajao kao otpadak pri Leblankovom procesu. Nakon oksidacije kalcijum-sulfida na vazduhu, proizvod bi se ispirao sa rastvorom natrijum-karbonata, a potom se nakon isparavanja vršila kristalizacija natrijum-tiosulfata[5]:
- 4CaS + 3H2O + O2 → 3Ca(OH)2 + Ca2S2O3 + 2S
- Ca2S2O3 + Na2CO3 → Na2S2O3 + CaCO3
U novije vreme se natrijum-tiosulfat proizvodi iz tečnosti koje predstavljaju otpatke pri proizvodnji natrijum-sulfida. Takva tečnost sadrži sulfid, sulfat, sulfit i karbonat. Pri koncentrovanju, ove soli se talože, da bi se onda procedile, rastvorile u vodi i napokon se tretiraju gasovima iz peći koji sadrže sumpor-dioksid[5]:
- 2Na2S + Na2CO3 + 4SO2 → 3Na2S2O3 + CO2
- 2Na2S + Na2SO4 + 3SO2 → 3Na2S2O3
Fizičko-hemijske osobine
Gradi krupne kristale u obliku pentahidrata koji se u vodi lako rastvaraju. Pri zagrevanju se raspada na natrijum-sulfat i natrijum-pentasulfid[5]:
- 4Na2S2O3 → Na2S5 + 3Na2SO4
Značaj
- Dejstvom razblažene mineralne kiseline na natrijum-tiosulfat izgleda da se gradi tiosumporna kiselina koja se raspada na sumpor-dioksid i elementarni sumpor:
- Na2S2O3 + 2HCl → 2NaCl + SO2 + S + H2O
Vreme nastanka sumpora zavisi od koncentracije rastvora. Ova reakcija se koristi za kvalitativno dokazivanje tiosulfata.
- U rastvoru sa jodom nastaje natrijum-jodid i natrijum-tetrationat:
- 2Na2S2O3 + I2 → 2NaI + Na2S4O6
Ova reakcija se mnogo primenjuje u volumetrijskoj analizi, ne samo za određivanje joda, već i ma kojeg oksidacionog sredstva koje oslobađa jod iz jodida, što znači za određivanje hlora, broma, bakarnih soli, hipohlorita i hlornog kreča.[5]
Izvori
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846. edit
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594. edit
- ↑ 5,0 5,1 5,2 5,3 5,4 Parkes, G.D. & Phil, D. 1973. Melorova moderna neorganska hemija. Naučna knjiga. Beograd.
Spoljašnje veze

- p
- r
- u
NaAlO2 • NaBH3(CN) • NaBH4 • Na2B4O7 10 H2O • NaBr • NaBrO3 • NaCH3COO • NaCFH2COO • NaHCOO • NaCN • NaC6H5CO2 • NaC6H4(OH)CO2 • NaC18H35O2 • NaCl • NaClO • NaClO2 • NaClO3 • NaClO4 • NaF • NaH • NaHCO3 • NaH2PO4 • Na2HPO4 • Na3PO4 • NaHSO3 • NaHSO4 • NaI • NaIO3 • NaIO4 • NaMnO4 • NaNH2 • NaNO2 • NaNO3 • NaN3 • NaOH • NaO2 • NaPO2H2 • NaReO4 • NaSCN • NaSH • NaTcO4 • NaVO3 • Na2CO3 • 2 Na2CO3 3 H2O2 • Na2C2O4 • Na2CrO4 • Na2Cr2O7 • Na2MnO4 • Na2MoO4 • Na2O • Na2O2 • Na2O(UO3)2 • Na2S • Na2SO3 • Na2SO4 • Na2S2O3 • Na2S2O4 • Na2S2O5 • Na2S2O6 • Na2S2O7 • Na2S2O8 • Na2Se • Na2SeO3 • Na2SeO4 • Na2SiO3 • Na2Te • Na2TeO3 • Na2Ti3O7 • Na2U2O7 • NaWO4 • Na2Zn(OH)4 • Na3N • Na3P • Na3VO4 • Na4Fe(CN)6 • Na5P3O10 • NaBiO3






