Bicarbonato de potássio
| Bicarbonato de potássio Alerta sobre risco à saúde | |
|---|---|
 | |
| Nome IUPAC | carbonato de potássio e hidrogênio |
| Outros nomes | carbonato ácido de potássio |
| Identificadores | |
| Número CAS | 298-14-6 |
| PubChem | 516893 |
| Propriedades | |
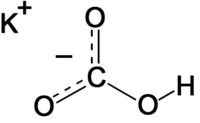
| Fórmula molecular | KHCO3 |
| Massa molar | 100.115 g/mol |
| Aparência | cristais incolores ou pó branco |
| Densidade | 2.17 g/cm3, sólido |
| Ponto de fusão | 292 °C |
| Solubilidade em água | 32.2 g/100 ml (20 °C) |
| Solubilidade | praticamente insolúvel em álcool |
| Acidez (pKa) | 8.2 (0.1M) |
| Estrutura | |
| Estrutura cristalina | monoclínico |
| Riscos associados | |
| MSDS | Potassium bicarbonate |
| Índice UE | Não listado |
| NFPA 704 |  0 1 0 |
| Ponto de fulgor | Não inflamável |
| Compostos relacionados | |
| Outros aniões/ânions | Carbonato de potássio Bissulfato de potássio Hidrogenofosfato de potássio |
| Outros catiões/cátions | Bicarbonato de sódio Bicarbonato de amônio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Bicarbonato de potássio (também conhecido como hidrogeno carbonato de potássio ou carbonato ácido de potássio), é uma substância salina, cristalina, na forma de um pó macio quando finamente pulverizado, de incolor a branca, inodora, levemente básica.
Tem número CAS [298-14-6].
Aplicações
O composto é usado como um fonte de dióxido de carbono, como fermento químico, em panificação, extinção de fogo com pó (extintores de incêndio), atuando como um reagente e um forte agente tamponador em medicações. É usado como uma base em alimentos para regular o pH.
Nas suas aplicações como fermento químico, e até como regulador de pH, atua devido a sua reação com ácidos (como o ácido tartárico), comportando-se como uma base, liberando dióxido de carbono:
- KHCO3 + H+ → K+ + H2O + CO2↑
Decomposição desta substância ocorre entre 100°C e 120 °C em K2CO3 (carbonato de potássio), H2O (água), e CO2 (dióxido de carbono),[1] o que é útil na sua aplicação como extintor de chamas, devido a liberação de dióxido de carbono e água:
- 2 KHCO3 → K2CO3 + H2O + CO2↑
Bicarbonato de potássio é solúvel em água, e é frequentemente adicionado a água engarrafada para alterar sabor; entretanto, não é solúvel em álcool. Em concentrações maiores que 0.5%, KHCO3 pode ter efeitos fitotóxicos em plantas (bicarbonato de potássio tem uso amplo em colheitas, especialmente para neutralização de solos ácidos), embora não haja qualquer evidência de carcinogenicidade em humanos, nenhum efeito adverso pela super-exposição, e nenhuma dosagem LD50.
Obtenção
É produzido pela reação do carbonato de potássio com dióxido de carbono e água:
Ou ainda resulta da simples dissolução do carbonato de potássio em água (embora tal reação não seja utilizada em sua produção industrial):
- K2CO3 + H2O → KHCO3 + KOH
História
A palavra saleratus, do Latim sal æratus significando "sal aerado", foi largamente usada no século XIX para tanto o bicarbonato de sódio quanto o de potássio. O termo foi posteriormente abandonado.
Referências
- ↑ POTASSIUM BICARBONATE - MSDS - www.jtbaker.com
Ligações externas
- «Potassium Bicarbonate Handbook» (PDF) (em inglês)
- «Potassium Bicarbonate: Crops» (PDF) (em inglês)
Ver também
 | Este artigo sobre um composto inorgânico é um esboço. Você pode ajudar a Wikipédia expandindo-o. |










