Arsenigzuur
| Arsenigzuur | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
 | ||||
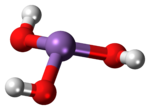 | ||||
| Algemeen | ||||
| Molecuulformule | ||||
| Andere namen | Triwaterstofarseniet | |||
| Molmassa | 125,94 g/mol | |||
| SMILES | O[As](O)O | |||
| InChI | 1/AsH3O3/c2-1(3)4/h2-4H | |||
| CAS-nummer | 13464-58-9 | |||
| PubChem | 545 | |||
| Wikidata | Q423271 | |||
| Beschrijving | Bestaat alleen in waterige oplossing | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H331 - H301 - H410 | |||
| Evenwichtsconstante(n) | pKz1 = 9,23 pKz2 = 13,52 | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Arsenigzuur is een oxozuur. Het is het arseen-analoog van fosforigzuur. De stof komt voor in waterige oplossingen, maar is niet als zuivere stof beschreven, hoewel het daarmee geen onbelangrijke component is.[1]
Properties
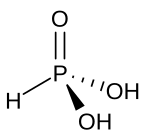
is een pyramidaal molecuul dat voornamelijk bestaat in de vorm waarin drie hydroxyl-groepen aan arseen gebonden zijn. Het 1H-NMR van arsenig zuur bestaat uit een enkel signaal, wat in overeenstemming is met de grote mate van symmetrie die in het molecuul aanwezig is..[2] Dit gegeven contrasteert sterk met de analoge fosfor-verbinding die voornamelijk voorkomt als , waarbij juist de -vorm slecht een zeer klein deel van de moleculaire populatie vormt. Het verschil in gedrag tussen arseen en fosfor is in overeenstemming met de algemene trend in het periodiek systeem, dat voor de lichtere elementen in een groep de hogere valenties stabieler zijn dan voor de zwaardere elementen.[3]
Het tautomere arsonzuur is, net als arsenigzuur niet als zuivere stof bekend.
Synthese
De bereiding van verloopt via een langzame hydrolyse van arseen(III)oxide in water. Toevoegen van een base zet het gevormde arsenigzuur om in arseniet-ionen , en .
Reacties
Met zijn eerste pKz- waarde van 9.2 is een zeer zwak zuur.[3] Reacties die toegeschreven zijn aan waterige arseen(III)oxide-oplossingen zijn die van arsenig zuur en zijn geconjugeerde basen.
Net als arseen(III)oxide reageert arseigzuur soms amfoteer. Met de waterstofhalogenides reageert tot de overeenkomstige trihalogenides:
De reactie van arsenigzuur met joodmethaan geeft methylarseenzuur. Deze, historisch, belangrijke reactie staat bekend als de Meyer-reactie:[4]
De alkylering vindt plaats op arseen en het oxidatiegetal van arseen gaat van +3 naar +5.
Toxicologie
Arseenhoudende verbindingen zijn zeer giftig en carcinogeen. De anhydride-vorm van het zuur, arseen(III)oxide, wordt gebruikt als herbicide, pesticide en rodenticide.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Arsenous acid op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Externe link
- Case Studies in Environmental Medicine - Arsenic Toxicity
Verwijzingen in de tekst
- ↑ Munoz-Hernandez, M.-A. (1994). "Arsenic: Inorganic Chemistry". In King, R. B. (ed.). Encyclopedia of Inorganic Chemistry. Chichester: John Wiley & Sons.
- ↑ Kolozsi, A., Lakatos, A., Galbács, G. (2008). A pH-Metric, UV, NMR, and X-ray Crystallographic Study on Arsenous Acid Reacting with Dithioerythritol. Inorganic Chemistry 47 (9): 3832–3840. PMID: 18380458. DOI: 10.1021/ic7024439.
- ↑ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ G. Meyer (1883). Ueber einige anomale Reaktionen. Berichte der Deutschen Chemischen Gesellschaft 13: 1439–1443. DOI: 10.1002/cber.188301601316.























