Asid klorik
 | |
 | |
| Nama | |
|---|---|
| Nama lain asid klorin(V) | |
| Pengecam | |
No. Pendaftaran CAS |
|
Imej model 3D Jmol |
|
| ChemSpider |
|
| ECHA InfoCard | 100.029.303 |
| Nombor EC |
|
PubChem CID |
|
| UNII |
|
| Nombor PBB | 2626 |
CompTox Dashboard (EPA) |
|
InChI
| |
SMILES
| |
| Sifat | |
Formula kimia | HClO3 |
| Jisim molar | 84.45914 |
| Rupa bentuk | larutan tidak berwarna |
| Ketumpatan | 1 g/mL (kira-kira) |
Keterlarutan dalam air | >40 g/100 ml (20 °C) |
| Keasidan (pKa) | kira-kira −1 |
| Struktur | |
| Bentuk molekul | 三角锥 |
| Bahaya | |
| Bahaya-bahaya utama | pengoksidaan |
| Sebatian berkaitan | |
Anion lain | asid bromik、asid iodik |
Kation lain | ammonium klorat、natrium klorat、 kalium klorat |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| Rujukan kotak info | |
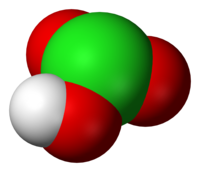
Asid klorik ialah sejenisoksiasid klorin yang ada formula kimia HClO3.Dalam oksiasid ini,keadaan pengoksidaan klorin ialah +5.Asid klorik adalah keasidan yang kuat(pKa≈−1) dan pengoksidaan kuat.Asid klorik boleh menghasilkan klorat.
Menghasilan
Ia boleh dihasilkan dengan mereaksikan barium klorat dan asid sulfurik:
- Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4
atau memanaskan asid klorus untuk merebutkan ia:
- 3HClO → HClO3 + 2 HCl
Lihat juga
- asid hipoklorus,asid klorus,asid perklorik
- asid bromik,asid iodik
Rujukan
- Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (ed. 2nd), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4CS1 maint: multiple names: authors list (link)
- King, R. B. (Ed.) (1994) Encyclopedia of Inorganic Chemistry, Vol. 2, p. 658. Chichester:Wiley. ISBN 0-471-93620-0
Templat:Klorat









