Tétraoxyde d'uranium
| Tétraoxyde d'uranium | |
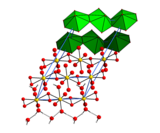 | |
| Identification | |
|---|---|
| No CAS | 12036-71-4 |
| No ECHA | 100.031.671 |
| No CE | 234-852-1 |
| SMILES | O1[U](O1)(=O)=O PubChem, vue 3D |
| InChI | InChI : vue 3D InChI=1/O2.2O.U/c1-2;;;/q-2;;;+2/rO4U/c1-5(2)3-4-5 |
| Apparence | solide cristallin jaune clair |
| Propriétés chimiques | |
| Formule | O4UUO4 |
| Masse molaire[1] | 302,026 5 ± 0,001 2 g/mol O 21,19 %, U 78,81 %, |
| Propriétés physiques | |
| T° fusion | décomposition à 200 °C |
| Précautions | |
 Composé radioactif | |
| SGH[2] | |
   Danger H300 : Mortel en cas d'ingestion H330 : Mortel par inhalation H373 : Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H411 : Toxique pour les organismes aquatiques, entraîne des effets à long terme | |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
Le tétraoxyde d'uranium, également appelé peroxyde d'uranium, voire peroxyde d'uranyle, est le composé chimique de formule UO4. C'est un solide jaune clair, soluble, qu'on trouve sous une forme hydratée UO4·nH2O, avec n compris entre 0 et 4. La solubilité du tétraoxyde d'uranium dépend très largement de son degré d'hydratation.
Pour n au moins égal à 2, UO4·nH2O peut également s'exprimer selon UO3·H2O2·(n-1)H2O, ce qui explique ses propriétés très similaires à celles du trioxyde d'uranium hydraté UO3·nH2O.
Le tétraoxyde d'uranium intervient comme intermédiaire dans le procédé d'enrichissement de l'uranium pour produire les barres de combustible MOX des centrales nucléaires.
Seuls deux minéraux d'uranyle sont connus à ce jour pour contenir du tétraoxyde d'uranium :
- la studtite UO4·4H2O
- la métastudtite UO4·2H2O
Articles liés
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a et b Entrée « Uranium compounds » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 14 septembre 2011 (JavaScript nécessaire)
v · m | |||
|---|---|---|---|
| U(II) |
| ||
| U(III) |
| ||
| U(IV) |
| ||
| U(IV,V) |
| ||
| U(V) |
| ||
| U(V,VI) |
| ||
| U(VI) |
| ||
| U(VIII) |
| ||
| U(XII) |
| ||
v · m | |
|---|---|
| États divers |
|
| État d'oxydation +1 |
|
| État d'oxydation +2 |
|
| État d'oxydation +3 |
|
| État d'oxydation +4 |
|
| État d'oxydation +5 |
|
| État d'oxydation +6 |
|
| État d'oxydation +7 |
|
| État d'oxydation +8 |
|
| Sujets connexes |
|
 Portail de la chimie
Portail de la chimie  Portail du nucléaire
Portail du nucléaire












 Tétraoxyde_d'uranium
Tétraoxyde_d'uranium