Tétrachlorure de dibore
| Tétrachlorure de dibore | |
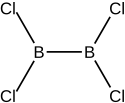 | |
| Structure du tétrachlorure de dibore | |
| Identification | |
|---|---|
| No CAS | 13701-67-2 |
| PubChem | 139548 |
| SMILES | B(B(Cl)Cl)(Cl)Cl PubChem, vue 3D |
| InChI | Std. InChI : vue 3D InChI=1S/B2Cl4/c3-1(4)2(5)6 Std. InChIKey : LCWVIHDXYOFGEG-UHFFFAOYSA-N |
| Propriétés chimiques | |
| Formule | B2Cl4 [Isomères] |
| Masse molaire[1] | 163,434 ± 0,022 g/mol B 13,23 %, Cl 86,77 %, |
| Propriétés physiques | |
| T° fusion | −93 °C[réf. nécessaire] |
| T° ébullition | 65 °C[réf. nécessaire] |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
Le tétrachlorure de dibore est un composé chimique de formule B2Cl4. Il s'agit d'un liquide incolore soluble dans l'eau en donnant de l'acide borique B(OH)3 et de l'acide chlorhydrique HCl.
- B2Cl4 + 6 H2O → 2 B(OH)3 + H2 + 4 HCl(aq).
Comme les autres tétrahalogénures de bore, il se décompose à température ambiante[2] à une vitesse qui s'accélère sous l'effet catalytique des produits de la décomposition :
- B2Cl4 → 1⁄n (BCl)n + BCl3.
Le tétrachlorure de dibore s'enflamme spontanément au contact de l'air :
- 6 B2Cl4 + 3 O2 → B2O3 + 8 BCl3.
Il fixe facilement l'hydrogène H2 à température ambiante[3] :
- 3 B2Cl4 + 6 H2 → 2 B2H6 + 4 BCl3.
Il peut être obtenu en faisant réagir du trichlorure de bore BCl3 avec du mercure ou du cuivre en présence de décharges électriques :
- 2 BCl3 + 2 Hg → B2Cl4 + Hg2Cl2.
- 2 BCl3 + 2 Cu → B2Cl4 + CuCl.
Cette réaction peut être divisée en trois étapes[3] :
- 2 BCl3 → 2 BCl2 + 2 Cl ;
- 2 Cl + 2Hg(électrode) → Hg2Cl2 ;
- 2 BCl2 → B2Cl4.
Il peut être utilisé comme précurseur dans la synthèse de composés organiques du bore, par exemple en réagissant avec l'éthylène C2H4[4] :
- CH2=CH2 + B2Cl4 → Cl2B–CH2–CH2–BCl2.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Ullmann's Fine Chemicals, John Wiley & Sons, 2013, p. 351, (ISBN 978-3-527-68357-4).
- ↑ a et b (en) Grant Urry, Thomas Wartik, R. E. Moore et H. I. Schlesinger, « The Preparation and Some of the Properties of Diboron Tetrachloride, B2Cl4 », Journal of the American Chemical Society, vol. 76, no 21, , p. 5293-5298 (DOI 10.1021/ja01650a010, lire en ligne)
- ↑ (en) Grant Urry, James Kerrigan, Theran D. Parsons et H. I. Schlesinger, « Diboron Tetrachloride, B2Cl4, as a Reagent for the Synthesis of Organo-boron Compounds. I. The Reaction of Diboron Tetrachloride with Ethylene », Journal of the American Chemical Society, vol. 76, no 21, , p. 5299-5301 (DOI 10.1021/ja01650a011, lire en ligne)
v · m Composés du bore | |||
|---|---|---|---|
| Pnictogénures |
| ||
| Halogénures |
| ||
| Acides |
| ||
| Boranes |
| ||
| Borates |
| ||
| Oxydes |
| ||
| Sulfures |
| ||
| Carbures |
| ||
| Composés organoborés |
| ||
| Borures |
| ||
| Borohydrures |
| ||
| Autres |
| ||
v · m | |
|---|---|
| Chlorures Cl(-I) |
|
| Interhalogènes | |
| Composés BCl4, AuCl4 |
|
| Composés AlCl6, PCl6... |
|
| Composés NbCl7, TaCl7 |
|
| Perchlorocarbures |
|
| Hydrocarbures halogénés |
|
| Oxohalogénures | |
 Portail de la chimie
Portail de la chimie












 Tétrachlorure_de_dibore
Tétrachlorure_de_dibore