Électrode standard à hydrogène

Pour les articles homonymes, voir ESH.

Une proposition de fusion est en cours entre Électrode normale à hydrogène et Électrode standard à hydrogène.
Les avis sur cette proposition sont rassemblés dans une section de Wikipédia:Pages à fusionner. Les modifications majeures apportées, entre-temps, aux articles doivent être commentées sur la même page.
Vous venez d’apposer le modèle {{à fusionner}}, suivez ces étapes :
| 1. | Apposez le bandeau sur les autres pages à fusionner :
| Utilisez ce texte : |
|---|---|---|
| 2. | Important : ajoutez une section dans Pages à fusionner en motivant votre proposition. | Pour créer la section : Créer la section sur la page des Pages à fusionner |
| 3. | Pensez à informer les contributeurs principaux de la page et les projets associés lorsque cela est possible. | Utilisez ce texte : |
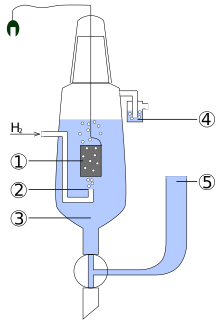
L'électrode standard à hydrogène (ESH) est l'électrode de référence absolue. Elle ne peut être réalisée en pratique. La réalisation pratique de l'ESH est l'électrode normale à hydrogène ou ENH.
L'ESH est une électrode où a lieu la réaction d'oxydation suivante :
- H2 ⇔ 2 H+ + 2 e−.
Cette réaction est réalisable mais l'ESH implique les suppositions suivantes :
- aH+ = aH2 = 1 ;
- γH+ = γH2 = 1,
où a représente l'activité chimique des différentes espèces et γ leur coefficient d'activité.
Ces suppositions reviennent donc à considérer que, pour réaliser une ESH, la réaction d'oxydation du dihydrogène devrait avoir lieu avec :
- une pression partielle PH2 égale à 1 bar ;
- une concentration en H+ égale à 1 mol/L ;
- le dihydrogène se comportant comme un gaz parfait ;
- le coefficient d'activité du proton γH+ égal à 1.
Les deux premiers critères peuvent être vérifiés. On obtient alors une électrode normale à hydrogène. Les deux seconds critères ne peuvent être vérifiés. C'est pourquoi l'ESH ne peut être réalisée.
Le caractère à part de l'ESH vient de la convention thermodynamique suivante : on a fixé arbitrairement le potentiel standard des protons en solution comme étant nul à toute température : μH+ = 0.
v · m Électrodes en chimie analytique | |
|---|---|
| |
| Électrode de référence | |
| Électrode de travail | |
| |
 Portail de la chimie
Portail de la chimie










