Oxid rhoditý
| Oxid rhoditý | |
|---|---|
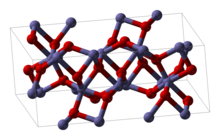 Krystalová struktura | |
| Obecné | |
| Systematický název | Oxid rhoditý |
| Anglický název | Rhodium(III) oxide |
| Německý název | Rhodium(III)-oxid |
| Sumární vzorec | Rh2O3 |
| Vzhled | tmavě šedý prášek žlutý prášek (pentahydrát) |
| Identifikace | |
| Registrační číslo CAS | 12036-35-0 |
| Vlastnosti | |
| Molární hmotnost | 253,8092 g/mol |
| Teplota rozkladu | 1 100 °C |
| Hustota | 8,20 g/cm3 |
| Rozpustnost ve vodě | nerozpustný |
| Rozpustnost v polárních rozpouštědlech | kyseliny zásady |
| Měrná magnetická susceptibilita | 5,127×10−6 cm3g−1 |
| Struktura | |
| Krystalová struktura | šesterečná (<750 °C) kosočtverečná (>750 °C) amorfní |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −286 kJ/mol |
| Bezpečnost | |
 GHS03  GHS07 Nebezpečí[1] | |
Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). Některá data mohou pocházet z datové položky. | |
Oxid rhoditý (Rh2O3) je oxidem rhodia, které je v něm přítomno v oxidačním stavu III.
Výroba
- Reakcí rhodia a hydroxidu sodného za přítomnosti hydrogensíranu draselného:
Rh + 3 NaOH → Rh(OH)3 + 3 Na
Použití
Nejvíce oxidu rhoditého se používá na výrobu katalyzátorů.
Reference
V tomto článku byl použit překlad textu z článku Rhodium(III) oxide na anglické Wikipedii.
- ↑ a b Rhodium(III) oxide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Literatura
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
 | Tento článek je příliš stručný nebo postrádá důležité informace. Pomozte Wikipedii tím, že jej vhodně rozšíříte. Nevkládejte však bez oprávnění cizí texty. |
Portály: Chemie









