Fluorid strontnatý
| fluorid strontnatý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Fluorid strontnatý |
| Anglický název | Strontium fluoride |
| Německý název | Strontiumfluorid |
| Sumární vzorec | SrF2 |
| Vzhled | bezbarvá pevná látka bez zápachu [1] |
| Identifikace | |
| Registrační číslo CAS | 7783-48-4 |
| EC-no (EINECS/ELINCS/NLP) | 232-000-3 |
| PubChem | 82210 |
| SMILES | [Sr+2].[F-].[F-] |
| InChI | InChI=1S/2FH.Sr/h2*1H;/q;;+2/p-2 Key: FVRNDBHWWSPNOM-UHFFFAOYSA-L |
| Vlastnosti | |
| Molární hmotnost | 125,62 g/mol |
| Teplota tání | 1,473 °C (2,683 °F; 1,746 K) |
| Teplota varu | 2,460 °C (4,460 °F; 2,730 K) |
| Hustota | 4,24 g/cm3 |
| Index lomu | 1,4380 |
| Rozpustnost ve vodě | špatně rozpustný (0,117 g/l při 18 °C) |
| Struktura | |
| Krystalová struktura | kubická |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −1217 kJ/mol |
| Bezpečnost | |
 GHS07 | |
| H-věty | H315, H319, H332, H335 |
| P-věty | P261, P264, P264+265, P271, P280, P302+352, P304+340, P305+351+338, P317, P319, P321, P332+317, P337+317, P362+364, P403+233, P405, P501[2] |
| Teplota vzplanutí | nehořlavé |
Některá data mohou pocházet z datové položky. | |
Fluorid strontnatý je anorganická sloučenina s chemickým vzorcem SrF2. Je to křehká bílá krystalická látka, která se vzácně v přírodě vyskytuje jako minerál.[3]
Příprava
Fluorid strontnatý lze připravit rozpuštěním uhličitanu strontnatého v přebytku 40% kyseliny fluorovodíkové:[4]
SrCO3 + 2HF → SrF2 + H2O + CO2
Fluorid strontnatý lze také připravit reakcí chloridu strontnatého s fluorem:
SrCl2 + F2 → SrF2 + Cl2
Struktura
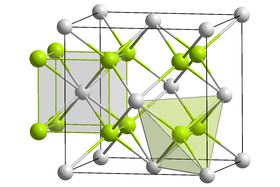
Pevný fluorid strontnatý má strukturu stejnou jako fluorit. V plynné fázi je molekula lomená s úhlem F-Sr-F přibližně 120°.[5] Jedná se o výjimku z teorie VSEPR, která předpokládá lineární strukturu.
Vlastnosti
Fluorid strontnatý je téměř nerozpustný ve vodě. Dráždí oči a kůži a je škodlivý při vdechnutí nebo požití. Podobně jako fluorid vápenatý a fluorid barnatý vykazuje fluorid strontnatý při zvýšených teplotách superiontovou vodivost.[6] Fluorid strontnatý je propustný pro elektromagnetické záření v rozsahu vlnových délek od ultrafialového záření (150 nm) po infračervené záření (11 µm). Jeho optické vlastnosti jsou na střední úrovni ve srovnání s fluoridem vápenatým a fluoridem barnatým.[7]
Využití
Fluorid strontnatý se používá například jako optický povlak na čočkách a také jako krystal termoluminiscenčního dozimetru.
Dále se využívá jako nosič radionuklidu stroncia-90 v radioizotopových termoelektrických generátorech.
Reference
V tomto článku byly použity překlady textů z článků Strontium fluoride na anglické Wikipedii a Strontiumfluorid na německé Wikipedii.
- ↑ GESTIS-Stoffdatenbank. gestis.dguv.de [online]. [cit. 2023-07-22]. Dostupné online. (německy)
- ↑ PUBCHEM. Strontium fluoride. pubchem.ncbi.nlm.nih.gov [online]. [cit. 2023-07-22]. Dostupné online. (anglicky)
- ↑ Strontiofluorite [online]. [cit. 2023-07-22]. Dostupné online.
- ↑ GEORG, Brauer; KWASNIK, W. Handbook of Preparative Inorganic Chemistry. 2. vyd. New York: ACADEMIC PRESS, 1963. 1858 s. Dostupné online. Kapitola Strontium Fluoride, s. 234.
- ↑ GREENWOOD, N. N.; EARNSHAW, A. Chemistry of the Elements. [s.l.]: Butterworth-Heinemann, 1997. ISBN 978-0-08-037941-8. (anglicky)
- ↑ Newmet Koch - Strontium. web.archive.org [online]. 2005-12-14 [cit. 2023-07-22]. Dostupné v archivu pořízeném z originálu dne 2005-12-14.
- ↑ Strontium Fluoride (SrF2) Optical Material. www.crystran.co.uk [online]. [cit. 2023-07-22]. Dostupné online.
| Anorganické soli strontnaté | |
|---|---|
| Halogenidy a pseudohalogenidy | |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlornan strontnatý (Sr(OCl)2) • Chloritan strontnatý (Sr(ClO2)2) • Chlorečnan strontnatý (Sr(ClO3)2) • Chloristan strontnatý (Sr(ClO4)2) • Bromičnan strontnatý (Sr(BrO3)2) • Jodičnan strontnatý (Sr(IO3)2) • Jodistan strontnatý (Sr(IO4)2) • Siřičitan strontnatý (SrSO3) • Síran strontnatý (SrSO4) • Dithionan strontnatý (SrS2O6) • Seleničitan strontnatý (SrSeO3) • Selenan strontnatý (SrSeO4) • Telluričitan strontnatý (SrTeO3) • Telluran strontnatý (SrTeO4) • Dusnan strontnatý (Sr(NO)2) • Dusitan strontnatý (SrNO2) • Dusičnan strontnatý (SrNO3) • Dihydrogenfosfornan strontnatý (Sr(H2PO2)2) • Hydrogenfosforitan strontnatý (SrHPO3) • Dihydrogenfosforitan strontnatý (Sr(H2PO3)2) • Fosforečnan strontnatý (Sr3(PO4)2) • Hydrogenfosforečnan strontnatý (SrHPO4) • Dihydrogenfosforečnan strontnatý (Sr(H2PO4)2) • Difosforečnan strontnatý (Sr2P2O7) • Metafosforečnan strontnatý (Sr(PO3)2) • Diarsenitan strontnatý (Sr2As2O5) • Metaarsenitan strontnatý (Sr(AsO2)2) • Hydrogenorthoarseničnan strontnatý (SrHAsO4) • Diarseničnan strontnatý (Sr2As2O7) • Antimoničnan strontnatý (Sr(Sb2O3)2) • Uhličitan strontnatý (SrCO3) • Šťavelan strontnatý (Sr(CO2)2) • Křemičitan strontnatý (SrSiO3) • Cíničitan strontnatý (SrSnO3) • Orthoolovičitan strontnatý (Sr2PbO4) • Titaničitan strontnatý (SrTiO3) • Zirkoničitan strontnatý (SrZrO3) • Železan strontnatý (SrFeO4) • Chroman strontnatý (SrCrO4) • Dichroman strontnatý (SrCr2O7) • Trichroman strontnatý (SrCr3O10) • Molybdenan strontnatý (SrMoO4) • Wolframan strontnatý (SrWO4) • Uranan strontnatý (SrUO4) • Manganistan strontnatý (Sr(MnO4)2) • Orthovanadičnan strontnatý (Sr3(VO4)2) • Metavanadičnan strontnatý (Sr(VO3)2) • Peroxovanadičnan strontnatý (Sr(VO4)2) • Boritan strontnatý (Sr(BO2)2) • Hlinitan strontnatý (Sr(AlO2)2) |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydrid strontnatý (SrH2) • Hydroxid strontnatý (Sr(OH)2) • Oxid strontnatý (SrO) • Peroxid strontnatý (SrO2) • Hydrogensulfid strontnatý (Sr(SH)2) • Sulfid strontnatý (SrS) • Azid strontnatý Sr(N3)2) • Amid strontnatý Sr(NH2)2) • Imid strontnatý SrNH) • Nitrid strontnatý Sr3N2) • Fosfid strontnatý (Sr3P2) • |









